Retranscription traduite (et raccourcie!) du All In Podcast, Episode 39. Disponible en Anglais ici.
Dre Nicola Sykes
Bonjour à toutes. Nous sommes ravis de retrouver aujourd’hui Docteure Chrisandra Shufelt, avec qui nous nous sommes entretenues pour la première fois dans l’épisode 28. Dre Shufelt a récemment rejoint la Mayo Clinic de Jacksonville, en Floride, où elle est présidente de la division de médecine interne générale et directrice associée du Women’s Health Research Center. Dre Shufelt est une interniste spécialisée dans la santé des femmes, qui a suivi une formation en biologie vasculaire et en santé des femmes, et qui est praticienne certifiée en ménopause. Ses recherches, financées par les National Institutes of Health (NIH) Americain, portent sur les jeunes femmes souffrant d’aménorrhée hypothalamique et évaluent l’impact sur la santé immunitaire et vasculaire, un sujet très pertinent pour nous toutes. Nous sommes ravis de vous retrouver, Chrisandra!

Dre Chrisandra Shufelt, Mayo Clinic Floride
Florence Gillet
Alors quand vous avez parlé à Nicola en 2022, c’est un des rares épisodes auquel je n’ai pas participé malheureusement – épisode 28, que j’invite vraiment nos auditeurices à réécouter. Mais c’est très agréable de vous rencontrer enfin. Pourriez-vous nous donner un résumé de ce dont nous avons parlé la première fois que nous vous avons rencontrée en 2022 ?
Dre Chrisandra Shufelt
En 2022, nous avions terminé une étude à Los Angeles où nous avions recruté des femmes atteintes d’AH et nous les avions comparées à des sujets sains, ce que nous appelons des témoins normaux, ce qui signifie simplement qu’elles ont leur cycle menstruel tous les mois, parce que nous voulions comparer les femmes qui avaient un taux d’œstrogène très bas, pas de cycles menstruels, à des femmes qui avaient des cycles menstruels réguliers et examiner leur santé osseuse, cardiaque et immunitaire. Nous avons fait appel aussi à un troisième groupe de femmes qui avaient naturellement perdu de l’œstrogène. Il s’agit de femmes récemment ménopausées.
Nous avons donc constitué un groupe de 30 femmes atteintes d’AH, 30 femmes ayant des cycles menstruels réguliers et 30 femmes récemment ménopausées. Aucune d’entre elles ne pouvait suivre un traitement hormonal. Nous voulions que tout soit sur un pied d’égalité. Nous avons mesuré la santé vasculaire, la santé osseuse et la santé immunitaire dans les trois groupes.
Ce que nous avons constaté très tôt, c’est que la santé vasculaire était affectée chez les femmes atteintes d’AH. Nous verrons un peu plus tard ce que cela signifie exactement. La santé osseuse aussi. Nous savons que les os sont fragilisés chez les femmes atteintes d’AH, mais il est intéressant de noter que la santé osseuse (lombaire) de ces femmes était exactement la même que celle d’une femme de 52 ans.
Nous avons également constaté une augmentation de l’inflammation. Mon hypothèse était que les femmes atteintes d’AH auraient plus d’inflammation et de problèmes vasculaires que le groupe témoin parce qu’elles n’ont pas d’œstrogènes, et nous savons que les œstrogènes favorisent l’oxyde nitrique, qui ouvre les vaisseaux sanguins.
La surprise, c’était que je pensais qu’elles seraient très semblables aux femmes ménopausées qui n’ont pas d’œstrogènes naturellement et en fait, les résultats vasculaires des femmes en AH étaient pires!
Il n’est donc pas bon de se promener sans œstrogènes dans la vingtaine ou la trentaine. Par contre, l’absence d’œstrogènes dans la cinquantaine, qui est une transition naturelle et normale vers la ménopause, ne vous expose pas forcément à des problèmes vasculaires à l’avenir. Voilà donc un aperçu de ce que nous avons découvert, et c’était une étude passionnante. Elle nous a permis d’obtenir le financement suivant des NIH pour étudier comment cela pourrait être un marqueur d’une maladie vasculaire.
Dre Nicola Sykes
C’est vraiment intéressant à savoir. Vous avez donc été l’auteure principal d’une étude récemment publiée en 2023, qui s’intéresse aux signaux précliniques de maladies cardiovasculaires chez les femmes atteintes d’AH. Vous avez mesuré l’indice hyperémique réactif (IHR) pour mesurer la fonction endothéliale. Pouvez-vous nous expliquer ce que cela signifie en termes simples ?
Dre Chrisandra Shufelt
Il s’agit d’un indice de dilatation et de constriction des vaisseaux sanguins de l’ensemble du corps, du cerveau et du cœur. Qu’est-ce qui contrôle l’ouverture et la fermeture de nos vaisseaux sanguins ? Par exemple, si votre rythme cardiaque augmente, vous avez besoin d’un flux sanguin plus important, vous vasodilatez. Ce qui contrôle cela, c’est la cellule qui tapisse tous les vaisseaux sanguins, la cellule interne appelée endothélium. Elle n’est épaisse que d’une seule cellule. C’est elle qui contrôle votre corps et qui vous dit, ok, maintenant nous avons besoin d’ouvrir et nous pouvons ouvrir ce vaisseau.
C’est ce qui se passe pendant l’activité physique. Nous savons que les œstrogènes peuvent agir sur cette paroi cellulaire et lui donner un signal de vasodilatation ou d’ouverture. C’est donc devenu l’hypothèse de travail ou la compréhension de ce qui se passe chez les femmes qui ont un faible taux d’œstrogènes. C’est donc l’un des tests que nous avons effectués. Et nous pouvons mesurer cela à l’aide d’un brassard de pression artérielle et de deux appareils qui se placent au bout de vos doigts, des méthodes non invasives.
Florence Gillet
Dans l’étude, vous avez constaté que 35 % des femmes atteintes d’AH avaient une fonction endothéliale qui était à un niveau associé à une future maladie cardiovasculaire. Selon vous, combien de temps faudrait-il avant de constater d’autres effets et que pourrait-il se passer ?
Dre Chrisandra Shufelt
Oui, c’est vrai. À notre grande surprise, nous avons trouvé un signal de DYSfonctionnement endothélial. La fonction endothéliale est une artère saine et normale qui s’ouvre et se ferme, s’ouvre et se ferme. Je compare cela à un élastique. Le dysfonctionnement endothélial est le fait que vos vaisseaux sanguins s’ouvrent et se ferment, mais qu’ils ne le font pas très bien. C’est un peu comme si vous trouviez un vieil élastique. Vous commencez à l’étirer et vous vous dites que vous pourriez l’utiliser, mais il n’est pas de bonne qualité. Puis, si vous attendez un an, vous retrouvez le même élastique dans ce tiroir. Il est peut-être devenu complètement sec et inutilisable. Or, nous savons que le dysfonctionnement endothélial est le premier de la cascade qui peut conduire aux maladies cardiaques. Et il n’est pas bon d’avoir un dysfonctionnement endothélial dans la vingtaine, car nous savons que 10 à 15, voire 20 ans plus tard, on peut développer une maladie cardiaque. Les jeunes femmes et les femmes d’âge mûr sont donc exposées à des risques.
Mais la bonne nouvelle, c’est que nous pouvons l’identifier, et que le dysfonctionnement endothélial, bien qu’il soit le premier domino de la cascade, est réversible. C’est donc une bonne nouvelle. Je pense donc que ce que je retiens ici, c’est que nous avons trouvé un signal indiquant que l’élastique n’est pas aussi extensible, mais qu’il est temps de réfléchir à la manière dont nous pouvons l’inverser, car cela ne signifie pas que vous êtes destinée à souffrir d’une maladie cardiovasculaire. Comme souffrir d’ostéopénie/ostéoporose ne signifie pas non plus que vous êtes destinée à avoir une fracture. Il s’agit simplement d’une prise de conscience.
Et comprendre que cette maladie n’affecte probablement pas qu’un seul système ! Nous savons qu’elle n’affecte pas seulement les ovaires. Elle n’affecte pas seulement les os. Nous nous intéressons maintenant au cœur. Et nous savons que cela peut avoir un impact sur l’humeur. Un impact sur la fertilité. Il s’agit donc probablement d’une maladie plus complexe. L’impact va bien au-delà de l’os.
Je pense donc que si nous avons identifié qu’un tiers des femmes atteintes de cette pathologie présentaient un dysfonctionnement endothélial, l’objectif est désormais de comprendre qui, parmi les personnes atteintes d’AH, présente ce dysfonctionnement endothélial. S’agit-il des plus stressées ? S’agit-il de celles qui font du sport à outrance ? S’agit-il de celles qui ne mangent pas assez et souffrent de troubles de l’alimentation ? Est-ce dû à la perte de poids ? Ou s’agit-il d’une combinaison de tous ces facteurs ?
Je pense que c’est ce qui rend l’AH si compliquée, si peu étudiée, si peu reconnue, parce que les médecins ne posent pas de questions sur toutes ces pathologies. Mais nos recherches se concentrent désormais sur les personnes qui souffrent d’AH. Car si nous pouvons dire, d’accord, les plus touchées sont celles qui font du sport de façon excessive, alors nous pourrons commencer à élaborer des lignes directrices pour dire : si vous avez une personne qui fait du sport de façon excessive, il faut examiner son cœur. Est-ce que ce sont les personnes qui ont des os plus fragiles ? Une femme passe une scintigraphie osseuse à 20 ans parce qu’elle a eu une fracture. Ses os sont fragilisés. Il faut maintenant examiner leur cœur. C’est donc un signal important pour nous dire qui est dans la population la plus à risque.
Florence Gillet
Cette étude a également mis en évidence l’association entre un taux élevé de cortisol et le manque d’élasticité des vaisseaux sanguins. Et vous avez dit que le problème était pire chez les femmes souffrant d’AH que chez celles qui ont connu une ménopause naturelle. Mais pouvez-vous également nous en dire plus sur l’impact d’un taux élevé de cortisol, donc d’hormones de stress, sur la fonction endothéliale dont vous avez parlé ?

Dre Chrisandra Shufelt
Oui. Et je pense que c’est de la plus haute importance parce que cela nous montre que l’AH n’est pas seulement une question d’œstrogènes mais un souci complexe. Elle peut se répercuter sur le cerveau. L’une des voies qu’elle ferme est l’accès hypothalamique, hypophysaire et ovarien. L’autre voie qu’elle régule à la hausse est l’accès aux glandes surrénales, qui fabriquent le cortisol, l’hormone du stress. En petites doses, le cortisol est nécessaire et important : il combat l’inflammation et permet de lutter contre les infections. Mais lorsque le cortisol est élevé pendant une période prolongée, il fait donc plus de tort que de bien. C’est pourquoi, alors que les œstrogènes favorisent cette doublure cellulaire de l’élastique qui peut s’ouvrir et s’étirer et qui favorise l’oxyde nitrique, le cortisol agit dans la direction opposée. Il s’agit donc presque d’une théorie à deux volets, selon laquelle l’œstrogène n’est pas le seul facteur en cause. Et nous le prouvons avec, si vous regardez les femmes sans cycles menstruels de l’AH comparées à celles sans cycles menstruels de la ménopause, la ménopause n’a toujours pas de dysfonction endothéliale. C’est donc probablement plus qu’une seule hormone, l’œstrogène. Il s’agit plutôt d’une théorie à deux ou même trois pans. Peut-être est-ce l’insuline, peut-être est-ce le cortisol, peut-être est-ce cette combinaison de deux ou trois facteurs.
Et peu importe que ce soit à cause du stress, de l’exercice physique, de troubles alimentaires ou d’une perte de poids. Le thème commun est que tout le monde a un taux de cortisol élevé.
Un taux élevé de cortisol dans un contexte de faible taux d’œstrogène est une très mauvaise combinaison, tandis qu’un faible taux d’œstrogène dans un contexte de ménopause n’est pas une mauvaise combinaison, car c’est une situation naturelle normale.
Mais encore une fois, je pense qu’il faut aller plus loin et comprendre comment ces facteurs interagissent mais, encore une fois, c’est compliqué et ce n’est pas seulement une question d’œstrogènes.
Dre Nicola Sykes
Lorsque nous avons discuté pour la première fois avant de commencer l’enregistrement, vous nous avez parlé des résultats de l’étude que vous avez récemment publiée, dans laquelle vous avez remplacé les œstrogènes chez les femmes par de l’AH, et vous avez obtenu des résultats très surprenants. Pourriez-vous nous en dire un peu plus à ce sujet et nous expliquer comment cela affecte les niveaux élevés de cortisol en AH?
Dre Chrisandra Shufelt
Tout à fait. Et ce n’est pas du tout ce que j’avais imaginé. Je pensais que si les femmes n’avaient pas d’œstrogènes : Il fallait leur redonner de l’œstrogène sous forme bioidentique, c’est-à-dire de l’œstradiol, et c’est ce que nous utilisons dans le traitement hormonal substitutif, appelée œstrogène bioidentique. Attention, ce n’est pas comme ce que nous utilisons dans les pilules contraceptives parce que ce n’est pas assez fort pour empêcher la production d’un ovocyte.
Il s’agit donc d’une hormone similaire à celle que l’ovaire produit chaque mois. Ce que nous avons fait, c’est que nous avons pris ces 30 femmes atteintes d’AH et, à ce stade de l’étude, nous les avons tirées au sort pour qu’elles reçoivent un patch d’œstrogène ou un patch placebo. Et elles l’ont porté pendant 12 semaines en continu sans progestérone. Ces patchs ne sont pas conseillés par les prestataires de soins médicaux. Nous ne voulons pas administrer de l’œstrogène seul en continu. Mais chez ces femmes, la muqueuse utérine était si fine que nous pouvions nous contenter d’administrer de l’œstrogène pur.
D’un point de vue scientifique, nous voulions répondre à la question suivante : quel est l’effet de l’œstrogène pur ? Nous avons donc administré l’œstrogène en continu pendant 12 semaines. Chaque personne a noté le nombre de patchs qu’elle a changés. Il s’agissait d’un essai scientifique randomisé au cours duquel nous avons mesuré la santé vasculaire au début, à la sixième semaine, puis à la douzième semaine. N’oublions pas qu’il s’agit de femmes présentant un dysfonctionnement endothélial. C’est le cas d’un tiers d’entre elles. Et voici le roulement de tambour.
Nous avons démontré que le remplacement des œstrogènes sous forme bio identique n’améliorait pas la fonction vasculaire au bout de 12 semaines. Donc, encore une fois, cela fait écho au fait qu’il s’agit d’une perturbation complexe de la fonction vasculaire.
Les conséquences cardiovasculaires vont peut-être au-delà de la simple perte d’œstrogènes. C’est donc une surprise.
L’autre élément que nous avons examiné est le cortisol. Nous nous sommes dit que si nous donnions de l’œstrogène, cela pourrait peut-être modifier les niveaux de cortisol, car ces femmes en AH ont des taux de cortisol élevés et après 12 semaines d’œstrogènes par rapport à un placebo, il n’y avait pas de différence dans le taux de cortisol.
Les taux de cortisol n’ont donc pas changé non plus. On espérait donc que l’œstrogène aurait un effet anti-inflammatoire sur le cortisol, et que ce dernier baisserait peut-être au fur et à mesure que nous le traiterions. Mais ce n’est pas le cas. C’est donc l’affection sous-jacente (l’AH) qui est le véritable moteur.
Dre Nicola Sykes
Il faut donc en déduire que le traitement hormonal substitutif n’est pas aussi efficace que le rétablissement des cycles menstruels naturels.
Dre Chrisandra Shufelt
Tout à fait. C’est une excellente conclusion. Les lignes directrices de la Société endocrinienne, celles de 2015, indiquent cependant que si vous n’avez pas eu vos règles depuis six ou neuf mois, un essai d’œstrogènes transdermiques est indiqué pour la santé des os. Encore une fois, nous ne nous sommes pas intéressés à la santé des os, et nous devons donc tenir compte du fait qu’il y a plus d’un système en jeu. Nous nous sommes intéressés à la santé cardiaque. Il y a donc probablement un impact sur la santé des os, ce qui est une bonne chose si les femmes n’ont pas leurs règles, mais aussi sur la santé du cœur. Nous voulons qu’elles retrouvent leur cycle menstruel.
Dr Nicola Sykes
Ce que je me demande, c’est si l’on prend des œstrogènes et de la progestérone, est-ce que cela aurait un impact différent ?
Dre Chrisandra Shufelt
Re- roulement de tambour. Rappelez-vous, j’ai présenté les résultats de l’utilisation continue sur 3 mois pour des raisons de sécurité. Les deux dernières semaines de l’étude. Donc, entre la semaine 12 et la semaine 14, nous avons donné de l’œstrogène ET de la progestérone. En effet, si l’on se contente d’administrer des œstrogènes, la muqueuse utérine peut devenir très épaisse. Et même si ces femmes n’ont pas eu leurs règles depuis plus de deux ou trois ans, nous devions intégrer cette sécurité. Donc, si vous avez le patch placebo, vous avez la progestérone placebo. Si vous receviez le vrai patch, nous vous donnions de la progestérone.
Nous avons donc pu examiner [l’administration de progesterone] et nous n’avons pas constaté d’amélioration de la santé vasculaire.
Pour moi, ce n’est pas surprenant car la progestérone n’active pas vraiment l’élasticité des vaisseaux sanguins. C’est l’œstrogène qui favorise l’oxyde nitrique. Or, la progestérone est anti-inflammatoire, très fortement anti-inflammatoire. Cela pourrait donc jouer un rôle, mais ce n’est pas le cas, mais il ne s’agissait que de deux semaines sur les 12 semaines.
Dre Nicola Sykes
Très bien. Une autre chose que nous constatons, et nous en avons parlé dans le dernier podcast, l’épisode 28, qu’on vous invite toutes à réécouter. Un certain nombre de personnes avec lesquelles nous avons été en contact, qu’il s’agisse de clientes ou de groupes de soutien, présentent un taux de cholestérol total légèrement élevé. Dans l’étude que vous avez publiée en 2023, les personnes atteintes d’AH présentaient des taux légèrement plus élevés de 12 milligrammes par décilitre en moyenne. Mais ce n’était pas statistiquement significatif. Le cholestérol a-t-il un impact sur la fonction endothéliale ? Pourrait-il y avoir une corrélation entre un taux de cholestérol plus élevé et une élasticité moindre des vaisseaux?
Dre Chrisandra Shufelt
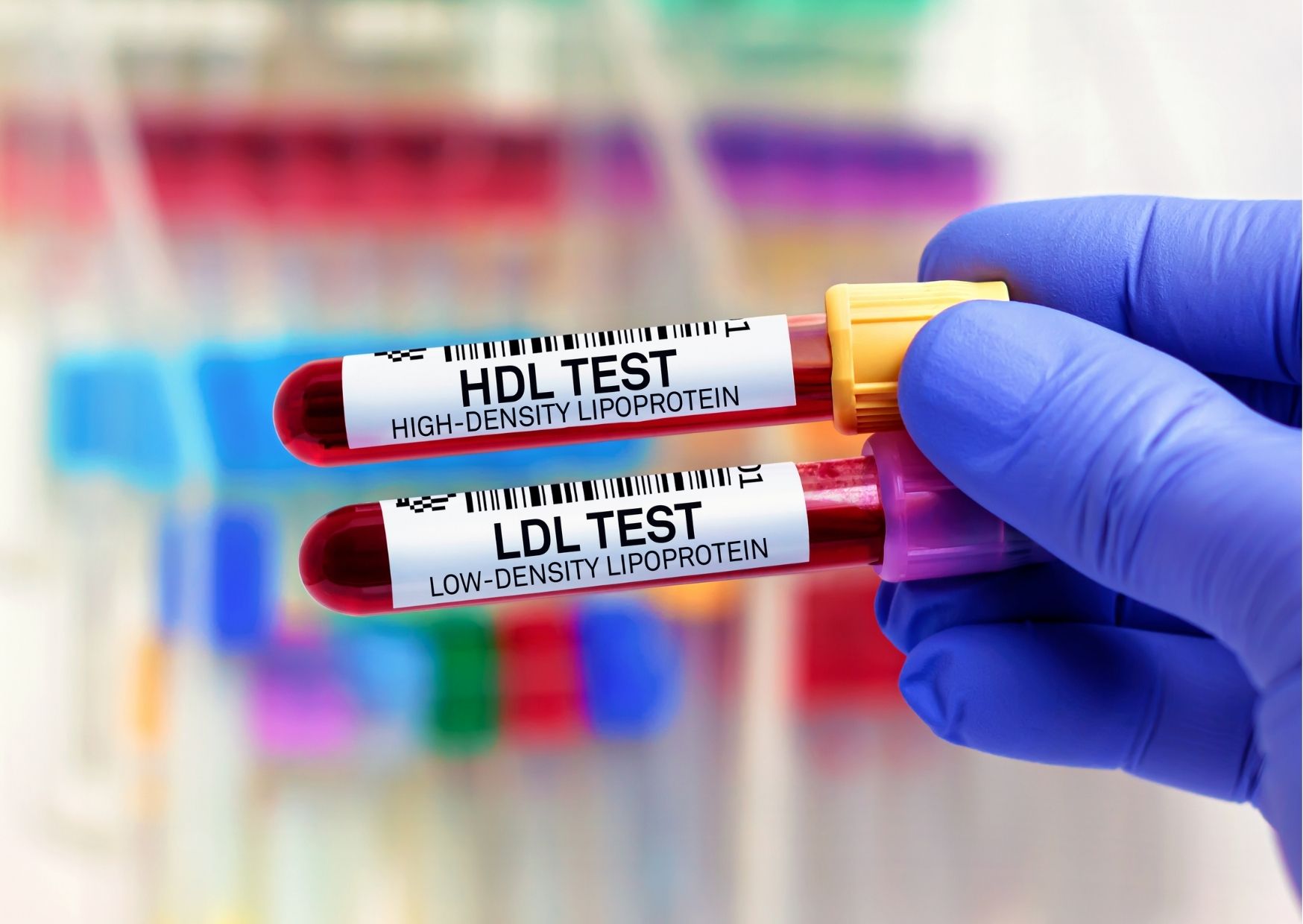
Tout à fait. C’est le cas, et cela a été démontré chez les femmes plus âgées dans des études plus importantes. Nous savons que l’œstrogène joue un rôle sur le « mauvais » cholesterol, le LDL. Nous savons également que les œstrogènes jouent un rôle sur le LDL.
Nous savons donc que les œstrogènes peuvent favoriser la diminution du LDL et l’augmentation du HDL, le bon cholestérol. Après la ménopause, on observe une augmentation du LDL et une diminution du HDL, et il s’agit d’une transition naturelle due à la perte d’œstrogènes. En revanche, dans le cas d’une perte brutale d’œstrogènes en AH, il serait logique de voir un changement pour le LDL et le HDL en raison de la faible quantité d’œstrogènes. Et le cortisol peut également jouer un rôle dans le cholestérol. Il peut faire basculer les choses dans la mauvaise direction. Encore une fois, il s’agit d’une théorie à deux volets, mais nous ne l’avons pas observée dans notre étude.
Je me suis entretenue avec des cardiologues très réputés qui sont des spécialistes des lipides. Notre prochaine idée est d’examiner les fractions des HDL et des LDL, car ces molécules sont de tailles différentes et pourraient jouer un rôle plus important. Bien que l’on observe une augmentation, nous n’avons pas constaté d’augmentation significative, mais on observe une élévation des LDL. Il se peut donc que le type de LDL que nous observons change. Et la fonction de la molécule pourrait également changer. Nous restons donc à l’écoute. C’est quelque chose que nous sommes en train d’approfondir : nous ne nous contentons pas de regarder les LDL et les HDL, qui ne sont que des composants, mais nous nous intéressons à la fonction et à la taille de chacun d’entre eux.
Florence Gillet
Vous avez mentionné dans l’autre épisode que, vous savez, la beauté de l’AH est qu’elle est absolument réversible. Donc je le rappelle pour les gens qui nous écoutent. Il est parfois très stressant d’entendre qu’il y a un impact direct sur la sante cardiaque, inflammatoire, osseuse, mais qu’il est également réversible.
Dre Chrisandra Shufelt
Complètement réversible.
Dre Nicola Sykes
Vous avez mentionné la grossesse. Lorsqu’une femme est enceinte, c’est une période où l’œstrogène est très élevé. Je pense donc que si une femme tombe enceinte peu de temps après sa guérison, j’espère que l’augmentation du volume sanguin due au fait d’être enceinte sera bénéfique. J’espère que le volume sanguin supplémentaire dû à la grossesse et à l’œstrogène sera utile dans ce cas.
Dre Chrisandra Shufelt
Tout à fait. Nous l’espérons. Mais ce dont nous voulons nous assurer, c’est que les femmes se soient rétablies avant de tomber enceintes, par opposition aux femmes qui ont encore une AH active et qui vont voir un médecin spécialiste de la fertilité pour recevoir des injections qui peuvent les rendre enceintes, parce que tant qu’elles ont une AH, elles sont infertiles. C’est une forme réversible d’infertilité. Soignons l’AH et nous résoudrons toutes ces choses que nous découvrons. Il y a deux types de choses différentes à considérer ici. La femme avec une AH active qui tombe enceinte par PMA par rapport à une femme qui s’est rétablie et qui est tombée enceinte. Je pense qu’il s’agit là de grossesses naturellement plus saines.
Dre Nicola Sykes
Pouvez-vous nous en dire un peu plus sur certains de vos derniers résultats dont vous avez parlé lors de conférences, mais qui n’ont pas encore été publiés ?
Dre Chrisandra Shufelt
L’autre grande découverte que nous avons pu présenter l’année dernière, lors du colloque sur la médecine de la reproduction, concerne les marqueurs d’inflammation. Nous avons comparé l’inflammation ou ce que nous appelons les cytokines. L’organisme a la capacité de favoriser l’inflammation en cas d’infection, lorsqu’il s’agit de se débarrasser d’un virus. Et nous savons que l’inflammation joue un rôle clé dans le dysfonctionnement endothélial. Par conséquent, si ces femmes – un tiers d’entre elles – présentent un dysfonctionnement endothélial, nous avons voulu examiner leur inflammation. Nous savons que les œstrogènes sont anti-inflammatoires et qu’ils peuvent donc réduire l’inflammation. Nous avons donc constaté que les femmes atteintes d’AH étaient comparées à des femmes qui avaient leurs cycles menstruels, au même âge et au même IMC.
Nous avons constaté que les femmes atteintes d’AH avaient des cytokines pro-inflammatoires plus élevées. Qu’est-ce que cela signifie ? Cela signifie qu’il s’agit de marqueurs d’inflammation dont on a constaté qu’ils entraînaient un dysfonctionnement endothélial.
Nous essayons donc maintenant de déterminer s’il s’agit de l’œuf ou de la poule. Et ce que je veux dire par là, c’est que ces femmes atteintes d’AH ont un taux de cortisol élevé, qu’elles ont une inflammation élevée et que cela conduit à un dysfonctionnement endothélial ? Ou bien le dysfonctionnement endothélial favorise-t-il l’inflammation, ou bien y a-t-il une dialectique entre les deux ?
Encore une fois, je ne peux que souligner la nécessité de poursuivre la recherche dans ce domaine. Si vous remontez à 2015, année où la Société endocrinienne a publié des lignes directrices sur l’AH. Ces lignes directrices sont louables, mais l’appel à la recherche y est très important. Leur conclusion était que nous avions besoin de plus de recherche. Donc, depuis 2015. Si l’on considère les recherches originales qui ont été menées, il s’agit de recherches scientifiques, comme l’essai clinique que j’ai mentionné avec le patch d’œstrogène, et non pas d’articles de synthèse, il y en a eu moins de 200. Moins de 200 ! Il n’est donc pas surprenant que les médecins ne sachent pas quoi faire avec cette maladie, parce qu’elle n’est pas étudiée. Et si vous regardez la même période, et je ne veux pas faire de comparaison parce qu’il s’agit de la santé des femmes, et je promeus la santé des femmes. Je suis un fournisseur de soins de santé pour les femmes, mais si vous regardez la même période pour le SOPK, il y a plus de 8 000 études sur le SOPK.
Dre Nicola Sykes
Wow.
Dre Chrisandra Shufelt
Il y a donc un déficit de recherche dans ce domaine, et c’est pourquoi je demande aux NIH de promouvoir et de soutenir cette recherche. C’est pourquoi nous avons besoin que les femmes s’inscrivent, parce que nous ne pourrons pas réaliser davantage d’études si nous n’avons pas de femmes qui s’inscrivent. C’est donc évidemment ma passion, parce que je veux obtenir les bonnes réponses.
Nous avons besoin de plus d’éducation. Parce que les médecins ne poseront pas de questions s’ils ne sont pas au courant de la maladie.
Florence Gillet
C’est vraiment le feedback que nous entendons le plus souvent, évidemment. Vous avez également mentionné que vous lanciez un nouveau registre pour les personnes atteintes d’une AH. Pouvez-vous nous en parler et nous dire comment les auditeurices peuvent y participer ? Y a-t-il des critères particuliers à remplir pour s’inscrire ?
Dre Chrisandra Shufelt
Tout à fait. C’est là que nous allons faire passer la recherche sur l’AH à la vitesse supérieure, car nous allons pouvoir répondre à un grand nombre des questions que nous soulevons en ce moment. L’objectif global est donc de créer un registre international. Nous l’appelons le registre « REVEAL » pour REgistry of Very Early estrogen loss and AnovuLation (registre de la perte d’œstrogène et de l’anovulation très précoces). Il s’agit donc d’un acronyme, car nous voulons révéler ce qui arrive aux femmes atteintes d’AH.
Nous mettons donc en place un registre de femmes diagnostiquées ou non, ou n’ayant pas de règles, atteintes d’AH, et nous avons besoin de comprendre la fréquence de ce problème menstruel. Nous devons connaître les diversités raciales et ethniques. Nous devons connaître la diversité des pays. Nous devons connaître les causes sous-jacentes, les facteurs de risque. Nous devons savoir ce qui se passe. Aussi pour la guérison !
Qu’est-ce que les femmes font qui fonctionne ? Et nous voulons vraiment connaître l’expérience globale de l’AH, y compris les symptômes, les soins qu’elles ont reçus, la manière dont elles recueillent leurs informations. Nous voulons vraiment savoir quel est l’impact sur leur travail, sur leurs études, leur structure sociale.
Nous allons également déterminer ce que nous appelons les déterminants sociaux de la santé. Je pense donc que ce sera l’occasion de répondre à toutes ces questions. Comment une femme peut-elle s’inscrire au registre ? Elle s’identifie elle-même comme ayant une AH ou comme ayant été informée. Nous lui demandons ensuite de signer le consentement par voie électronique, tout se faisant dans le confort de son domicile, pour autant qu’elle dispose d’un ordinateur. Pour l’instant, les questionnaires sont rédigés en anglais. Nous les traduirons bientôt en espagnol, puis dans d’autres langues, car pour avoir un impact mondial, nous devons, comme vous le savez, grâce à toutes les traductions de votre livre, les mettre à la disposition d’un très grand nombre de femmes. Et en même temps, ces femmes, si elles ne le savent pas, si elles n’ont pas vu de médecin, n’ont pas eu de règles depuis cinq mois. Et si elles répondent à ce questionnaire, nous soupçonnons qu’elles sont atteintes d’AH. Nous travaillons actuellement avec une société qui dispose d’une technologie de mesure des hormones à partir d’une goutte de sang. Nous leur enverrons donc un kit par la poste. Il suffit de recueillir un tout petit peu de sang. Ils le renvoient ensuite à la société et le font passer par un séparateur de sérum spécial et prioritaire. C’est un papier très sophistiqué. Nous pouvons obtenir leurs taux d’hormones et déterminer si c’est le diagnostic. Ensuite, elles feront partie du registre. Elles recevront un questionnaire qu’elles devront remplir en 10 ou 15 minutes. Les questionnaires seront donc les suivants : un questionnaire, à remplir en 10 ou 15 minutes, comprenant également un journal alimentaire de trois jours, recueillant toutes les informations alimentaires et nutritionnelles au tout début, puis au bout de trois mois, et ensuite, une fois par an. Vous recevez un questionnaire une fois par an. Il s’agirait donc d’un moyen de recueillir des informations de manière prospective et longitudinale (mots scientifiques, je sais), mais aussi de manière continue et de collecter des informations sur les expériences des femmes au dela du biais de la mémoire. Je pense donc qu’il s’agit d’une opportunité qui va vraiment changer l’empreinte de la recherche et qui va vraiment changer la compréhension de cette maladie et la façon dont nous pouvons former les médecins pour qu’ils en sachent plus.

Dre Nicola Sykes
C’est phénoménal. Je suis très enthousiaste. Je vais donc créer une URL pour les auditeurs : noperiod.info/reveal. S’il vous plaît, si vous écoutez et que vous avez une AH, allez sur noperiod.info/reveal et inscrivez-vous à ce registre. Je pense que c’est formidable. Je suis très enthousiaste. Merci beaucoup d’avoir partagé cela avec nous.
Dre Chrisandra Shufelt
Absolument. Merci à vous deux de promouvoir la compréhension et la sensibilisation, car c’est grâce à ce type de forums que davantage de femmes sont informées sur cette maladie, sur ce qu’il faut faire et sur la manière de se rassembler. Je suis la scientifique, je suis la médecine clinicienne qui fait de la recherche, mais ce que vous faites a un impact considérable parce que les femmes obtiennent les bonnes informations. Vous savez, je dis toujours en plaisantant que le Dr Google n’a pas de diplôme de médecine, et c’est vrai. Ne commencez pas à faire des recherches sur Google à propos de cette maladie, à moins que vous n’alliez sur des sites et des forums vraiment valables comme celui-ci.
Florence Gillet
C’est un honneur de vous recevoir et d’apporter les derniers résultats à nos auditeurs. Nous vous en sommes très reconnaissantes. Quel serait l’endroit idéal où envoyer les gens s’ils veulent prendre contact avec vous ?
Dre Chrisandra Shufelt
Je suis sur les médias sociaux, je suis sur Twitter, et je sais que beaucoup de médecins sont sur Twitter parce que nous aimons aller aux conférences et poster des diapositives et faire des commentaires. Mais je publie beaucoup de nos recherches sur Twitter. Il s’agit de @cshufeltMD. C’est là que je publie le plus d’informations sur les recherches en cours ou les conférences auxquelles je participe. Sinon, je le fais par le biais de notre prospectus d’étude. Et bien sûr, je suis sur le site de la Mayo Clinic.
Pour plus d’aide dans ta guerison, telecharge mon guide gratuit : se liberer de la peur de grossir en 5 etapes concretes ou reserve ta premiere seance de coaching a moins de 30 euro ici




